简介通用气体常数
理想气体状态方程:pV=nRT
已知标准状况(备注:0℃,1标准大气压)下,1mol理想气体的体积为22.4L
把p=101325Pa,T=273K,n=1mol,V=22.4L=0.0224m^3代进去
得到R=8.3138462≈8.314,单位J/(mol*K)
玻耳兹曼常数的定义就是k=R/Na
气体常数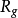 =R/M,
=R/M,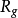 为所求气体的气体常数。R称为通用气体常数,也称普适气体恒量,不会随气体的分子量变化而改变。M为所求气体的摩尔质量,例如1mol氢气的
为所求气体的气体常数。R称为通用气体常数,也称普适气体恒量,不会随气体的分子量变化而改变。M为所求气体的摩尔质量,例如1mol氢气的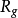 ,R为8.314,1mol氢气的M为0.002KG,则
,R为8.314,1mol氢气的M为0.002KG,则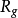 =8.314/0.002=4157J/(mol*K)2
=8.314/0.002=4157J/(mol*K)2
气体常数表征理想气体热力学特性的一个常数。 为理想气体的绝对压力p和比容v 的乘积与热力学温度T之比。常以 符号“R”表示,单位为“J/(kg·K)”。 气体常数在数值上即相当于质量 为1kg的理想气体在可逆定压 加热过程中温度每升高1K时对 外所作出的膨胀功。其值仅取决于 气体的种类,与气体所处的热力状 态无关。例如氧气的R总是等于 259.8J/ (kg·K)、氮气的R恒为 296.7J/(kg·K)等。在工程热力学 等学科中,常根据通用气体常数除 以千摩尔质量或按迈耶公式来计算确定各种理想气体的气体常数。3
数据
|| ||
相关推导补充R单位推导:
由理想气体状态方程:pV=nRT 得:R=pv/(nT) [其中各个量的单位 p: pa, v:m3, n: mol, T: k]
带入单位进行推导:R[]=pa*m3/(mol*k)(其中pa*m3可以拆分为: pa*m2*m,而由F=PS知道 pa*m2即为N牛顿单位,由W=FS知道,N*m即为功的单位 J)所以通过以上代换可以得到R的单位:J/(mol*k)
美国标准大气1976年美国标准大气局将气体常数R *定义为:
R * = 8.31432×103N m kmol-1 K-1。
注意使用千摩尔单位,导致常数中的因子为1000。 USSA1976承认该值与Avogadro常数和Boltzmann常数的引用值不一致。这种差异与准确性并不是显着的偏离,USSA1976将这个R *值用于标准气氛的所有计算。 当使用R的ISO值时,计算出的压力在11公里(相当于只有17.4厘米或6.8英寸的差异)上增加了0.62帕斯卡,而在20公里增加了0.292帕(相当于只有差异 0.338米或13.2英寸)。4




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国