五氟化碘(Iodine pentafluoride),一种卤素互化物,分子式为IF5,分子量为221.8965。
为无色液体,在空气中会发生烟雾。与可燃物及有机物接触能促进燃烧,并能够腐蚀玻璃。
碘的氟化物比碘元素单独存在时的反应性、刺激性、腐蚀性更强。与水或潮湿空气剧烈反应,放出剧毒和腐蚀性烟雾,吸入会中毒,对皮肤、 眼睛和黏膜有强烈刺激性和腐蚀性。
发现历史在1891年,五氟化碘首次由亨利·莫瓦桑(Henry Moissan)用碘与氟反应而制得。
莫瓦桑长期从事无机化学的研究,其中最为著名的是合成单质氟。他将经过干燥的碘与气态氟作用,碘在单质氟中迅速燃烧,生成一种密度较大的、无色透明的液体,这种液体能够与玻璃迅速地发生反应,并发出响声。他改变碘和氟的比例,使用过量的碘或过量的氟,发现产物没有变化。经过进一步的研究,发现这种液体是五氟化碘。在一百多年后的现今,该反应条件已经改良了,但这个放热反应仍被用来制成五氟化碘。
早在20世纪50年代初国外很多公司就开始研究五氟化碘的合成及应用,20世纪70年代后期,国外的公司已经对五氟化碘开始较全面的研究并逐步实现产业化。在国外,生产五氟化碘的主要公司有ABCR GmBR Co、空气产品与化学公司、索尔维氟化工公司、霍尼韦尔公司等。
国内氟化工起步较晚,20世纪70年代以前,为满足国防工业的需要,中国开始生产氟化物,但生产工艺基本上沿用前苏联的技术,工艺简单,设备落后,产品品种比较单一。80年代初期,在改革开放的新形势下,中国利用氟资源生产无机氟化物的厂家逐渐增多。早期对五氟化碘的制备研究也不多,随着我国全氟碘烷及含氟表面活性剂和织物整理剂的巨大需求和快速发展,氟化剂在氟塑料、氟橡胶、氟表面活性剂、医药领域应用越来广泛,氟系列产品的需求日益提高,市场前景良好。但由于含氟表面活性剂和含氟织物整理剂的高额利润,国外企业不愿单独销售全氟碘烷给中国。因此,为突破这种现状,已经有不少企业的科研人员开始进行科研探索。123
理化特性物理性质分子结构:四方锥
键长(I—F):轴向:184.4pm;赤道面:186.9pm
临界温度:300.2℃
临界压力:4290kPa
熔化热(9.4℃):50.5kJ/kg
气化热(104.5℃):39.32kJ/kg
生成焓(液态):ΔHfΘ = -882.0kJ/mol
生成自由能(液态):ΔGfΘ = -780.7kJ/mol
电导率(液体,25℃):5.4×10-6 Ω-1·cm-1
热容:0.447kJ/(kg·K) (气体,25℃);0.463kJ/(kg·K)(液体,25℃)
蒸气压:8.46kPa(42℃);21.24kPa (62℃);66.92kPa(92℃)45
化学性质五氟化碘的热稳定性较好,是最稳定的卤素间化合物。IF5的反应活性比其他卤素间化合物弱得多,与硅、镁、铜、铁、铬在常温下不发生作用,在强热时才与钼、钨、磷、砷、锑、硼等发生作用,生成相应的氟化物,如:
2 IF5 + 2 Sb → 2 SbF5 + I2
6 IF5 + 10 B → 10 BF3 + 15 I2
在水中能很快水解生成氢氟酸和碘酸:
IF5 + 3 H2O → HIO3 + 5 HF
IF5是一个很好的溶剂,具有如下自电离作用:
2 IF5 ⇌ IF4+ + IF6-
IF5作为溶剂时,KF·IF5是一种路易斯碱,SbF5、BF3、HF、SO3为路易斯酸,此两类物质间的中和反应同发生在BrF3中的情况类似:
KF + IF5 → K+ + IF6-
SbF5 + IF5 → IF4+SbF6- ⇌ IF4+ + SbF6-
晶体结构分析和振动光谱表明 IF5 同 SbF5 作用,生成了[IF4]+[SbF6]- 类型的化合物。碱金属氟化物和 IF5 能发生作用,生成了 M+IF6- 形式的固体衍生物,其中M为碱金属、Ag、NO等。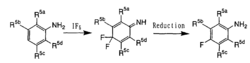
IF5在室温时,也会在富集的氢气中燃烧,但大多数的有机物同IF5发生较缓和的取代反应,CCl4能缓慢转化为CCl3F和CCl2F2,同四碘化碳、四溴化碳、二硫化碳、三氯乙酸和脂肪胺、酮、苯以及其他芳香化和物作用时,一般都是发生取代反应,但在某些情况下既能发生取代反应也能发生加成反应。
五氟化碘与伯胺反应,加水后水解形成腈:R-CH2-NH2 + IF5 → R-CF2-NH2 —H2O→ R-CN
参考资料:167
制备制备方法简介
氟气(用氮气稀释)通过碘上方:I2 + 5 F2 → 2 IF5
用I2与AgF、ClF3、BrF3、RuF2等氟化:3 I2 +5 AgF → 5 AgI + IF5
碘化氢或金属碘化物与氟作用:HI + 3 F2 → IF5 + HF
五氧化二碘与氟、三氟化氯、三氟化溴、四氟化硫等作用:2 I2O5 + 5 SF4 → 4 IF5 + 5 SO2
参考资料:78
固体碘在氟气中燃烧法
从生产状况来看,使用碘在氟气中燃烧的方法在充分做好安全措施的情况下是可行的,同时也是制备五氟化碘的主要方法。
制备步骤:
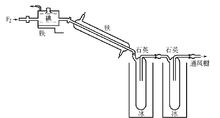
用有冷却套的鼓状铁筒作反应器(如图所示)。铁筒连接一个铁冷凝器,其后是两个石英制气体阱。
把碘装在反应器中,通入氟氮混合气(尽可能不含氟化氢)。氟氮混合气和液体碘在反应器内混合,氟气与碘发生合成反应,反应温度控制在 120~160℃,反应生成气态 IF5 。冷却水可将反应热带走,并使留在反应器中的 IF5 不变成 IF7 。当装置末端有F2逸出时,反应结束。停止冷却反应器,把水套作水浴,外面用煤气灯加热,在 F2 气流中将 IF5 蒸出,当氟电解槽的电流为80A时要使250g I2完全反应,约需10h(包括蒸馏时间),按碘计产率90%。91011
熔融态碘在氟气中燃烧法
熔融态碘与氟气的反应中,由于液体碘在反应器底部结晶,阻碍了反应器的换热,氟气与熔融状态的碘反应时反应速度快,放热量大,使得反应温度难以控制,且碘在高温时易产生大量碘蒸气,导致管道堵塞,同时温度过高,氟气与五氟化碘极易生成七氟化碘,导致收率降低和副反应偏高;连续通入反应器的大量氟气,其中过量 的氟气将造成很大浪费和污染,不符合清洁生产的要求;液态碘腐蚀性较大,对反应釜材质的要求较为苛刻。
John Theodore Lileck 等将固体碘置于镍反应器中经电加热线圈加热至高于114℃,得到熔融状态的碘;然后将氟气通过喷射器(喷射器放置在碘液面以下)均匀地分散在反应器中,在反应器下部鼓风冷却,反应器中的压力等于或大于五氟化碘的蒸气压,来阻止产物五氟化碘的挥发,以及减少副产物七氟化碘的生成。该工艺解决了反应中存在的上述管道堵塞以及副反应产物多等问 题,该工艺中五氟化碘的产率相对较高,以碘计高达 98%,以氟气计为 92%12
氟气处理烷基碘化物法
当用氟气处理烷基碘化物时,氟气会与之反应,生成碘的氟化物,以五氟化碘为主。该方法相对于碘在氟气中燃烧法要温和很多,但是该法的主要目的在于得到氟化后的氟碳化合物,五氟化碘只是作为副产物得到,数量较为有限,无论从原料成本还是产量来说都难以作为生产五氟化碘的主要方法。10
氟化银与碘单质反应法
该法是将 AgF 与 I2 混合,在适当的条件下使之反应,制取五氟化碘,理论上反应是可行的,但是考虑到氟化银的原料成本因素,该方法同上一种方法一样难以成为主要的制备方法。10
碘酸钾与四氟化硫反应法
William Channing Smith 等将 KIO3 与 SF4 的混合物阶梯式地加热保温使之反应后再分离得到 IF5 和 KIF6。 混合物先加热到60℃后保温2小时,再加热到120℃保温2小时,后又加热到140℃再保温4小时,最后加热到240℃保温6小时。收集反应生成的黄色挥发性组分,冷冻到-78℃,分离后加热到室温,所留下的液体即为五氟化碘。反应体系中的 KIO3 具有爆炸危险,因此操作过程中应当格外小心,尚未见到工业应用的报道。10
五氧化二碘与四氟化硫反应法
该方法是将 I2O5 在二氧化碳-丙酮混合物中冷却,抽真空到1mmHg,加人 SF4 后封闭,再进行阶梯式升温,后冷却分离,升温程序与上一种方法基本相同,产物分馏即可得到较高纯度的五氟化碘。该方法也尚未见到工业化的报道。781013
用途合成有机氟化物由于五氟化碘 (IF5)是一种稳定地、可储存的液体氟源,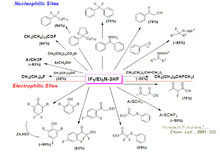 与其它氟发生联合的机会很少,因此可作为一种氟中间体来使用。五氟化碘作为一种通用的氟化剂和强氧化剂,在有机合成中具有重要的作用,如可用来制备合成全氟烷基碘化物的调聚剂五氟碘代乙烷:
与其它氟发生联合的机会很少,因此可作为一种氟中间体来使用。五氟化碘作为一种通用的氟化剂和强氧化剂,在有机合成中具有重要的作用,如可用来制备合成全氟烷基碘化物的调聚剂五氟碘代乙烷:
5 CF2=CF2 + IF5 + 2 I2 → 5 C2F5I
除此之外,五氟化碘还能与异硫氰代烷反应生成氟代烃的衍生物,以及合成其他含氟化合物等。
五氟化碘 (IF5) 很少用于氟化普通的有机化合物,这是由于难以控制其反应性。北海道大学教授 Yoneda 发现 IF5 与三乙胺三氢氟酸盐(Et3N·3HF)结合使用显著提高反应的选择性,使之成为一种低成本的过程和普遍适用的工业氟化技术,在各种含氟有机材料的工业合成中得以应用。使用IF5/Et3N·3HF 盐作为有机化合物的氟化试剂,对于亲核加成和亲电加成反应具有高度的选择性,各种有机合成方案如图所示。
文字及图片资料来源:81114
制作非水体系电池对于锂一卤素互化物非水电池体系的研究,国外文献中有过报道,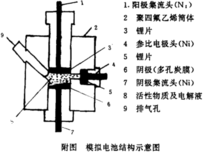 Park, KH 和 Miles MH 等人首次报道了用三氟化溴作为锂电池正极活性物质的试验结果。在国内,杨汉西、张克立等人对卤素互化物与锂构成的非水电池体系作过探索。结果表明,卤素互化物作为正极活性物质,可与锂构成高比能和开路电压的新一类锂电池体系。选用 IF5 为正极活性物质,对其构成的锂电电池体系进行研究,该电池体系的开路电压为4.45 V,电池在电流密度不大的情况下可进行工作,可望在实际中得到应用。
Park, KH 和 Miles MH 等人首次报道了用三氟化溴作为锂电池正极活性物质的试验结果。在国内,杨汉西、张克立等人对卤素互化物与锂构成的非水电池体系作过探索。结果表明,卤素互化物作为正极活性物质,可与锂构成高比能和开路电压的新一类锂电池体系。选用 IF5 为正极活性物质,对其构成的锂电电池体系进行研究,该电池体系的开路电压为4.45 V,电池在电流密度不大的情况下可进行工作,可望在实际中得到应用。
直接采用 IF5 为液体正极尚有困难。但可让其溶于具有良好导电性的溶剂中,而 IF5 只作正极活性物质来使用,则效果较好。由于IF5 的氧化性相当强,因此,选择溶剂时应注意,要求IF5 在溶剂中相当稳定,不与溶剂发生化学反应。选择溶质时,要求溶质在溶剂中有一定的溶解度,而且不与IF5 反 应。如LiBF4、LiAsF6、KPF6、LiClO4、Bu4NClO4 等在不同条件下,可不同程度地满足要求。此外,对IF5 的浓度也有一定要求,选择合适的浓度是影响 电池性能的因素之一。选择 POCl3 为溶 剂,Bu4NClO4 为电解质, 在该电解液中,可在一定的时间内稳定。将 Bu4NClO4 溶解到POCl3 中,配成含 Bu4NClO4 0.25 mol/L 的溶液,然后加入IF5 液体。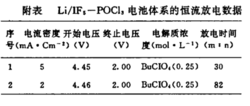
根据实验放电电压(4.45 V)以及热力学计算结果,电池反应应按照下列方程式进行:
10 Li + 2 IF5 → I2 + 10 LiF , EΘ = 4.40 V
实验结果为IF5 构成非水锂电池的可能性提供了依据。然而,POCl3 和 Bu4NClO4 并非是理想的溶剂及电解质,贮存性能差,怎样寻找理想 的溶剂和电解质,使电池在贮存过程中无副反应发生,是很有意 义的研究课题,有待人们进一步去探索。15
制备无机氟化物在无机氟化方面,五氟化碘现今最大的用途为含氟表面活性剂和防油防水纺织品处理剂生产中的原料,用于合成含氟表面活性剂和含氟织物整理剂的原料,也作为温和、易于操作的氟化剂,氟化某些金属。
IF5和HF组成体系是一种比IF5更优良的溶剂,可用来制备多种含氟的配合物。相比于其他卤素化合物,IF5 的反应活性较弱,但也能与许多金属及金属氧化物反应,如与五氧化二钒、五氧化二锑、三氧化钼、三氧化钨、三氧化铬和高锰酸钾在加热或煮沸情况下反应,相应地生成下列化合物:
2VOF3 · 3IOF3 , SbF5 · 3IO2F , 2MoO3 · 3IF5 , WO3 · 3IF5 , CrO2F2 和 MnO3F,如:
KMnO4 + IF5 → MnO3F + IOF3 + KF716
注意事项危险性概述危险性类别:第5.1类氧化剂
侵入途径:吸入 食入 经皮吸收
健康危害:对皮肤、眼睛和粘膜有强烈的刺激性和腐蚀性,与水或潮湿空气剧烈反应,放出剧毒和腐蚀性烟雾,吸入会中毒。遇热分解释出高毒的氟、碘烟雾。17
急救措施皮肤接触:用流动清水冲洗,涂敷氧化镁甘油软膏。就医。
眼睛接触:拉开眼睑,用流动清水冲洗15分钟。就医。
吸入:脱离现场至空气新鲜处。呼吸困难时给输氧。呼吸停止时,立即进行人工呼吸。就医。
食入:误服者,口服牛奶、豆浆或蛋清,就医。17
消防措施危险特性:强氧化剂。与易燃物、有机物接触易着火燃烧。与水能发生强烈反应。放出剧毒的腐蚀性烟雾。接触酸或酸气能产生有毒气体。
建规火险分级:甲
有害燃烧产物:氟化氢、碘化氢。
灭火方法:二氧化碳、干粉。不宜用水。17
接触控制及个体防护接触限值:美国TLV-TWA:2.5mg(F)/m3
工程控制:密闭操作,局部排风。
呼吸系统防护:可能接触其蒸气时,应该佩戴防毒口罩。紧急事态抢救或逃生时,建议佩戴自给式呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿相应的防护服。
手防护:戴防化学品手套。17
储存信息储存注意事项储存于阴凉、干燥、通风良好的库房。保持容器密封。防止受潮和雨淋。防止阳光曝晒。应与酸类、易燃物、可燃物、潮湿物品等分开存放。搬运时要轻装轻卸,防止包装及容器损坏。分装和搬运作业要注意个人防护。17
泄漏应急处理疏散泄漏污染区人员至安全区,禁止无关人员进入污染区,建议应急处理人员戴自给式呼吸器,穿化学防护服。不要直接接触泄漏物,禁止向泄漏物直接喷水,更不要让水进入包装容器内。用砂土吸收,铲入提桶,送至空旷地方,然后慢慢倒入大量水中,经稀释的污水放入废水系统。用水刷洗泄漏污染区,对污染地带进行通风。如果大量泄漏,回收。17
废弃处置废弃物性质:工作现场禁止吸烟、进食和饮水。工作后,淋浴更衣。工作服不要带到非作业场所,单独存放被毒物污染的衣服,洗后再用。车间应配备急救设备及药品。
其他有害作用:工作现场禁止吸烟、进食和饮水。工作后,淋浴更衣。工作服不要带到非作业场所,单独存放被毒物污染的衣服,洗后再用。车间应配备急救设备及药品。17
安全信息危险运输编码:UN 2491 5.1/PG 1
危险品标志:氧化剂
安全标识:S17S45S36/S37/S39
危险标识:R8R14R3418
计算化学数据1、疏水参数计算参考值(XlogP):3.6
2、氢键供体数量:0
3、氢键受体数量:5
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积:0
7、重原子数量:6
8、表面电荷:0
9、复杂度:37.1
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:119
本词条内容贡献者为:
包申旭 - 副教授 - 武汉理工大学资源与环境工程学院




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国