氰化溴,又名溴化氰,溴氰等。主要用于有机合成、炼金、制杀虫剂等。毒作用似氢氰酸,氰化氢,氰化钠,并有明显刺激性。吸入后引起头痛、头晕、恶心、呕吐、虚弱、惊厥、昏迷、咳嗽、呼吸困难,重者发生肺水肿,可致死。对眼和皮肤有强烈刺激性。另外,对于环境亦有很强的危害。
物性数据
1.性状:无色或白色针状或立方形结晶,常温下挥发。
2.熔点(℃):52。
3.沸点(℃):61.4。
4.相对密度(水=1):2.02(20℃)。
5.相对蒸气密度(空气=1):3.65。
6.饱和蒸气压(kPa):13.33(23℃)。
7.辛醇/水分配系数:-0.29。
8.溶解性:溶于水,易溶于乙醇、乙醚,溶于苯1。
分子结构数据
1、摩尔折射率:14.32。
2、摩尔体积(cm3/mol):51.6。
3、等张比容(90.2K):132.3。
4、表面张力(dyne/cm):43.2。
5、极化率(10-24cm3):5.67。
计算化学数据
1、疏水参数计算参考值(XlogP):1.1
2、氢键供体数量:0
3、氢键受体数量:1
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积:23.8
7、重原子数量:3
8、表面电荷:0
9、复杂度:31.3
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:12
性质与稳定性
1.具有强烈的吸湿性,对空气和湿气敏感,遇水会发生激烈反应放出氢气。
2.稳定性:稳定。
3.禁配物:强氧化剂、碱类。
4.避免接触的条件:受热、水蒸气。
5.聚合危害:聚合。
6.分解产物:溴化氢、氰化氢。
合成方法
1、制备溴化氰的装置如下图,在抽气良好的通风橱中将500g溴(160mL)装在一个用冰盐冷却剂冷却的IL磨口瓶中。加50mL水覆盖在溴上。在激烈搅拌下170g NaCN溶于1200mL水的溶液以每秒1滴的速度滴入。反应混合物的温度保持在20℃以下。要避免氰化物局部过量生成(CN)x。将最后的150mL NaCN溶液用水稀释至原体积的2倍,继续加溶液,每加一次要猛烈摇荡烧瓶。一旦摇荡时出现不再消失的棕色,即可弃去其余NaCN溶液(加NaCN约需5h)。把一个弯成V形的粗玻璃管装在圆底烧瓶上(如图)。在较短臂装颗粒状CaCl2,在水浴上将CNBr蒸出。产物聚集在作接受器用的广口瓶中,呈雪白的结晶,590g,按溴计产率90%。
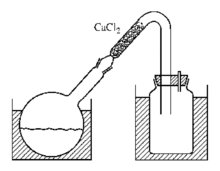
2、通过氰化钠或丙烯腈和溴制备而成。
贮存方法
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。包装要求密封,不可与空气接触。应与氧化剂、碱类、食用化学品分开存放,切忌混储。不宜大量储存或久存。储存应备有合适的材料收容泄漏物。
用途
1、溴化氰是一种常用的氰化试剂,在氰化反应领域,用途十分广泛,可以合成大量的氰化物。利用它也可以方便地生成多种具有生物活性的物质,诸如脲、硫脲、硒脲、胍盐、羟基胍盐和其它大量的杂环化合物等。
2、用于有机合成、炼金、制杀虫剂等2。
溴化氰活化
溴化氰活化法是常用的活化方法之一,活化过程主要是生成亚胺碳酸活性基团,它可以和伯氨基(NH2)反应,主要生成异脲衍生物。
溴化氰活化的基质可以在温和的条件下与配体结合,结合的配体量大。利用溴化氰活化的基质通过进一步处理还可以得到很多其它的衍生物。这种方法的缺点是溴化氰活化法的基质和配体偶联后生成的异脲衍生物中氨基的pKa=10.4,所以通常会带一定的正电荷,从而使基质可能有阴离子离子交换作用,增大了非特异性吸附,影响亲和层析的分辨率。另外溴化氰活化的基质与配体结合不够稳定,尤其是当与小配体结合时,可能会出现配体脱落现象。另外溴化氰有剧毒、易挥发,所以操作不便。
本词条内容贡献者为:
唐浩宇 - 教授 - 湘潭大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国