同一原子内由1个ns 轨 道 和 1个 np 轨道参与的杂化称为sp杂 化 ,所形成的两个杂 化轨道称为SP杂化轨道。每 个 sp 杂化轨道含有1/2的 S成 分 和 1/2的 p成分,杂化轨道 间的夹角为180°。sp轨道杂化是基于轨道杂化理论的一个重要分支,是一种比较常见的轨道杂化方式。
杂化过程以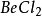 的形成过程为例说明sp杂化过程。基 态 Be的外层电子构型为2
的形成过程为例说明sp杂化过程。基 态 Be的外层电子构型为2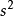 ,在成键时先发生激发,成为激发态2
,在成键时先发生激发,成为激发态2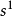 2
2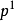 。随即发生 杂化,即 Be的1个2s 轨道和1个 2p 轨道进行sp杂化,形 成 两 个sp杂化轨道,每个杂化 轨道中各有一个未成对电子。两 个 Cl原子的3
。随即发生 杂化,即 Be的1个2s 轨道和1个 2p 轨道进行sp杂化,形 成 两 个sp杂化轨道,每个杂化 轨道中各有一个未成对电子。两 个 Cl原子的3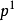 轨道以“头顶头”方式与各杂化轨道大 的一端重叠,形成两个σ键。由 于 Be的 两 个 sp杂化轨道间的夹角是180°,因此所形成 的
轨道以“头顶头”方式与各杂化轨道大 的一端重叠,形成两个σ键。由 于 Be的 两 个 sp杂化轨道间的夹角是180°,因此所形成 的 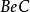
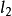 的几何构型为直线形。
的几何构型为直线形。 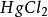 & II B 族元素的其他
& II B 族元素的其他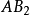 型直线型分子的形成与上述过程相似。1
型直线型分子的形成与上述过程相似。1
注意事项(1)原子轨道的杂化只有在形成分子的过程中才会发生;
(2)能量相近的原子轨道间才能发生杂化,能量相近通常是指:ns与np、ns,np与nd或(n-1)d。2
本词条内容贡献者为:
杨剑虹 - 教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国