马来酸恩替卡韦片,本品适用于病毒复制活跃,血清丙氨酸氨基转移酶(ALT)持续升高或肝脏组织学显示有活动性病变的慢性成人乙型肝炎的治疗。
警示语核苷类药物在单独或与其他抗逆转录病毒药物联合使用时,已经有乳酸性酸中毒和重度的脂肪性肝肿大,包括死亡病例的报道。
当慢性乙肝患者停止抗乙肝治疗后, 包括恩替卡韦在内,已经发现有乙肝严重急性加剧的报道。对那些停止抗乙肝治疗的患者肝功能应从临床和实验室检查等当面严密监测,并且至少随访数月。如必要,可重新恢复抗乙肝病毒的治疗。(见【警告】1.停止治疗后的肝炎加剧)。
有限的临床经验提示,如果恩替卡韦用于治疗慢性乙肝病毒(HBV)合并人类免疫缺陷病毒(HIV)感染且未经抗HIV治疗的患者,有可能出现对于HIV核苷逆转录酶抑制剂的耐药。在HBV合并HIV感染并且没有接受高效抗逆转录病毒治疗(HAART)的患者中,不推荐使用恩替卡韦(见【警告】3.合并感染HIV)。
成份主要活性成份:马来酸恩替卡韦。
化学名称:2-氨基-9-[(1S,3R,4S)-4-羟基-3-羟甲基-2-亚甲基环戊基]-1,9-二氢-6H-嘌呤-6-酮马来酸盐一水合物。
化学结构式: 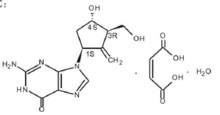

分子式:C12H15N5O3·C4H4O4·H2O
分子量:411.38
性状本品为薄胶衣片,除去包衣后显白色或类白色。
作用类别鸟嘌呤核苷类似物
适应症本品适用于病毒复制活跃,血清丙氨酸氨基转移酶(ALT)持续升高或肝脏组织学显示有活动性病变的慢性成人乙型肝炎的治疗。
规格0.5mg(以C12H15N5O3计)
用法用量患者应在有经验的医生指导下服用本品。
推荐剂量:
成人和16岁及以上的青少年口服本品,每天一次,每次0.5mg(一片)。拉米夫定治疗时发生病毒血症或出现拉米夫定耐药突变的患者为每天一次,每次1mg(两片)。
本品应空腹服用(餐前或餐后至少2小时).
肾功能不全
在肾功能不全的患者中,恩替卡韦的表观口服清除率岁肌酐清除率的降低而降低(参见药代动力学,特殊人群)。肌酐清除率10 x ULN和>2倍基线水平以外所有指标较基线值变差达3级或4级;
b A1463022和A1463027研究。
C包括A1463026和A1463014,A1463014研究是一个多国家的、随机双盲的Ⅱ期研究,该研究在使用拉米夫定治疗中复发病毒血症的患者中进行,这些患者或改力每日一次服用三种不同剂量的恩替卡韦(0.1,0.5和1.0mg),或继续每日一次服用100mg拉米夫定,持续52周。
d包括血常规、常规生化、肾功能和肝功能检查、胰酶和尿常规
e 3级=3+大量、≥500mg/dL;4级=4+,显著、严重
f 3级=3+大量;4级=≥4+,显著、严重、多量
ULN:正常值上限
在这些研究中,使用恩替卡韦的患者在治疗过程中发生ALT增高达1 0倍的正常值上限和基线值的2倍时,通常继续用药一段时阔,ALT可恢复正常;在此之前或同时伴随有病毒载量2个对数值的下降。故在用药期间,需定期检测肝功能。
停止治疗后的肝炎加剧(见【警告】)
肝炎急性加剧或ALT复燃的定义为:ALT大于10倍的正常值上限和大于2倍患者的参考水平(基线值或停药时最后一次检测值间的最小值)。所有停止治疗(无论何种原因)的患者中,出现了ALT复燃的患者例数均记录在表4中。这些研究中,如果在第52周或之后达到方案所规定的治疗应答后,可允许一亚组患者停药。如果未达到治疗应答而停用恩替卡韦则停药后发生ALT复燃的概率可能更高。

参考值是指基线或停药时最后一次检测值中的最小值。停药后恶化的中位时间对于恩替卡韦治疗的患者为23周,而对于拉米夫定治疗的患者为10周。
A1463038双盲研究中观察到,HBV合并感染HIV的患者接受恩替卡韦1 mg(N=51)或安慰剂(N=17)治疗24周,两组的安全性相似,并且与未合并感染HIV患者中观察到的安全性相似(见【警告】3:合并感染HIV)
禁忌对马来酸恩替卡韦或制剂中任何成份过敏者禁用。
注意事项肾功能不全的患者
肌酐清除率 肝移植受体患者
恩替卡韦及本品治疗肝移植受体的安全性和有效性尚不清楚。如果认为肝移植受体需要接受恩替卡韦治疗,其曾经或正在接受可能影响肾功能的免疫抑制剂,如:环孢菌素或他克莫司的治疗,应在本品给药前及给药过程中严密监测肾功能。(见【药代动力学】)
患者须知
患者应在医生的指导下服用本品,并告知医生任何新出现的症状及合并用药情况。应告知患者如果停药有时会出现肝脏病情加重,所以应在医生的指导下改变治疗方法。
患者在开始本品治疗前,需要进行HIV抗体的检测。应告知患者如果感染了HIV而未接受有效的HIV药物治疗,本品可能会增加对HIV药物治疗耐药的机会(见【警告】3.合并感染HIV)。
使用本品治疗并不能降低经性接触或污染血源传播HBV的危险性。因此,需要采取适当的防护措施。
孕妇及哺乳期妇女用药恩替卡韦及本品对妊娠妇女影响的研究尚不充分。只有当对胎儿潜在的风险-利益作出充分的权衡后,方可使用本品,
目前尚无资料提示本品能影响HBV的母婴传播,因此。应采取适当的干预措施以防止新生儿感染HBV。恩替卡韦可从大鼠乳汁分泌。但人乳中是否有分泌仍不清楚,所以不推荐服用本品的母亲哺乳。
儿童用药16岁以下儿童患者使用本品的安全性和有效性数据尚未建立。
老年用药由于没有足够的65岁及以上的老年患者参加本品的临床研究,尚不满楚老年患者与年轻愚者对本品的反应有何不同。恩替卡韦的临床试验报告也未发现者年患者与年轻患者之间的不
同。恩替卡韦主要由肾脏排泄,在肾功能损伤的患者中,可能发生毒性反应的危险性更高。因为老年患者多数肾功能有所下降,因此应注意药物剂量的选择,并且监测肾功能。
药物相互作用体内和体外试验评价了恩替卡韦的代谢情况。恩替卡韦不是细胞色素P450( CYP450)酶系统的底物、抑制剂或诱导剂。在浓度达到人体内浓度约10000倍时,恩替卡韦不抑制任何主要的人CYP450酶: 1A2、2C9、2C19、2D6、3A4、286和2E1。在浓度达到人体内浓度约340倍时,思替卡韦不诱导人CYP450酶: 1A2、2C9、2C19、3A4、3A5和2B6。同时服用通过抑制或诱导CYP450系统而代谢的药物对恩替卡韦的药代动力学没有影响。而且,同肘服用恩替卡韦对已知的CYP底物的药代动力学也没有影响。
研究恩替卡韦与拉米夫定、阿德福韦和替诺福韦的相互作用时,发现恩替卡韦和与其相互作用药物的稳态药代动力学均没有改变。
由于恩替卡韦主要通过肾脏清除,服用降低肾功能或竞争性通过主动肾小球分泌的药物的同时,服用恩营卡韦可能增加这两个药物的血药浓度。同时服用恩替卡韦与拉米夫定、阿德福
韦、替诺福韦不会引起明显的药物相互作用。同时服用恩替卡韦与其他通过肾脏清除或已知影响肾功能的药物的相互作用尚未研究。患者在同时服用恩替卡韦与此类药物时要密切监测不良反应的发生。
药物过量目前尚无使用本品过量的相关报道。在健康人群中恩替卡韦片单次给药达40毫克或连续14天多次给药20mg/天后,未观察到不良事件发生的增多。如果发生药物过量,须监测患者的 毒性指标,必要时进行标准支持疗法。
单次给药1mg恩替卡韦后,4个小时的血液透析可清除约13%的恩替卡韦。
药理毒理药理作用
微生物学
作用机制
本品为鸟嘌呤核苷类似物,对乙肝病毒(HBV)多聚酶具有抑制作用。它能够通过磷酸化成为具有活性的三磷酸盐,三磷酸盐在细胞内的半衰期为15小时。通过与HBV多聚酶的天然底 物三磷酸脱氧鸟嘌呤核苷竞争,恩替卡韦三磷酸盐能抑制病毒多聚酶(逆转录酶)的所有三种活性:(1) HBV多聚酶的启动;(2)前基因组mRNA逆转录负链的形成;(3) H8V-DNA正链的合成。恩替卡韦三磷酸盐对细胞的α、β、δ DNA多聚酶和线粒体y DNA多聚酶抑制作用较弱,K值为18至大于160μM。
抗病毒活性
在转染了野生型乙肝病毒的人类HepG2细胞中,恩替卡韦抑制50%病毒DNA台成所需浓度(EC50)为0.004 H M。恩替卡韦对拉米夫定耐药病毒株(rtL180M,rtM204V)的EC50的中位值是0.026 μM(范围0.01至0.059 μ M)。
恩替卡韦与HIV核苷逆转录酶抑制剂(NRTIs)联合给药,不太可能降低恩替卡韦的抗H8V疗效或后一类药物中任何一种药物的抗HIV疗效。细胞培养中检验HBV联合治疗,发现在大范围浓度内,阿巴卡韦,去羟肌昔,拉米夫定,司他夫定,替诺福韦或齐多夫定对患替卡韦的抗HBV活性均无拮抗作用。在HIV抗病毒活性实验中,当恩替卡韦浓度大于体内峰浓度4倍时,恩替卡韦对于6种NRTIs药物的细胞培养中的抗HIV活性无拮抗作用。
抗HIV病毒活性
全面分析恩替卡韦对一组实验室分离毒株以及临床分离的Ⅰ型人类免疫缺陷毒株( HIV-1)的抑制活性,在不同细胞及实验条件下获得的EC50值范围是0.026到>10μM;当病毒水平降低时观察到更低的EC50值。在细胞培养中,恩替卡韦在微摩尔浓度水平时可选择出HIV逆转录酶的M184I位点置换,在恩替卡韦高浓度水平时证实了抑制作用。含M184V位点置换的HIV变异株对恩替卡韦失去敏感性。
耐药性
细胞培养
位于逆转录酶区有rtM204I/V和rtL180M位点置换的拉米夫定耐药株(LVDr)对恩替卡韦的敏感性较HBV野毒株下降了8倍。合并其他恩替卡韦耐药氧基酸rtT184,rtS202和/或rtM250微店改变的,在细胞培养还发现,对恩替卡韦的敏感性降低。合并其他(rtT184A,C,F,G,I,L,M或S;rtS202C,G或I;和/或rtM250I,L或V)位点置换的临床分离株与野毒株相比,对恩替卡韦的敏感性进一步降低了16至741倍。单独出现rtT184,rtS202和rtM250恩替卡韦耐药位点置换的病毒株对恩替卡韦的敏感性仅有一定影响,在超过1000例没有拉米夫定耐药位点置换的患者中未观察到敏感性降低。细胞培养中发现,耐药性是通过改变HBV逆转录酶减少竞争结合而介导的,耐药的HBV毒株复制能力减弱。
临床研究中对初始接受恩替卡韦0.5mg(核苷初治)或1mg(拉米夫定失效)治疗,并且在治疗24周或之后,对于在治疗中做了HBV-DNA PCR检测的患者均进行了耐药监测。
核苷类药物初治患者:核苷类药物初治患者研究中,恩替卡韦长达144周治疗发现有rtT184、rt202和/或rtM250恩替卡韦耐药位点置换基因检测证据的患者比例




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国