亲电性,指某物质具有从其他分子或离子获得电子或与其他分子或离子分享电子的性质。有亲电试剂参与的反应,均为亲电子反应,如亲电子催化反应,即催化剂从反应物取得一对电子的催化作用;亲电子置换反应,即亲电子基团攻击和置换化合物中的敏感基团并在这个位置上和该化合物共价结合的反应。
亲电试剂指在化学反应中具有亲电性的化学试剂,可用E+表示。亲电试剂含有能够形成新的化合键的能量较低的空电子轨道。亲电试剂可以是中性的,也可以是电正性的。所谓亲电试剂是一种电子对受体,即路易斯酸。在反应过程中,它倾向于与电负性物种结合,因为电子是电负性的,所以“亲电”即是指亲“电负性”。
亲电试剂进攻亲核试剂上电子集中的部位。由这类亲电试剂进攻而发生发反应称为亲电反应。有机化学中常见的亲电子试剂有阳离子(如H﹢ 和 NO2﹢)、极性分子(如卤化氢、卤代烃、酰卤,和羰基化合物)、可极化中电性分子(如Cl2 和 Br2)、氧化剂(如有机过氧酸)、不具备八隅体电子的试剂(如卡宾和自由基)、以及某些路易斯酸(如 BH3 和 DIBAL)。其他亲电试剂还有有机磷化合物,碘代乙酸和环氧化物等,前者包括二异丙基氟磷酸和甲基氟磷酸异丙酯。
取代基的亲电性配体上有其它基团存在会影响配体的碱性,因而也影响形成配合物的稳定性。配体上的电子具有一定的活动性,当受其它基团影响时,电子云可发生转移。如甲基有排电子的能力,电子云在甲基的邻位或对位最大,使对位或邻位的酚基中的氢不容易离解,反映出它具有较大的pKa值,因而它形成配合物最稳定。相反,硝基、Br-均有吸电子能力,在它邻位或对位的氧上电子云密度减少,酚基中H+容易离解,因此它们生成配合物稳定性比起苯酚要小得多。1
但也可产生空间阻碍,使稳定性下降。在分析化学中常利用改变取代基来提高对某一金属离子的选择性,如8-羟基喹啉能与Al3+和Be2+生成难溶配合物。如果在2位上引入甲基,则由于产生空间位阻,不能与Al3+形成八面体配合物,而能与Be2+形成四面体构型的稳定配合物,所以2-甲基-8-羟基喹啉可用于Al3+和Be2+共存下的Be2+定量分析。
常见反应亲电性重排反应有机化合物中,羰基或其他吸电子基团(Electron-withdrawinggroup,EWG)或电负性较大的原子(如氧原子、氮原子)相连的α-碳原子上的氢县具有一定的酸性,可在强碱的作用下形成碳负离子。若分子内还含有其他缺电子性亲电基团的话,则可引起亲电性重排反应,生成相应的重排产物。
举例:Favorskii重排反应
a-卤代酮在碱的作用下重排生成羧酸或其衍生物的反应称为Favorskii重排反应,根据所用碱的不同(苛性碱、醇盐或胺),可分别得到羧酸、酯或酰胺。
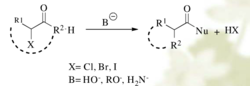
亲电性取代反应以苯环的亲电取代反应为例:
已知苯环平面的上下有π电子云结合较疏松,因此在反应中苯环可充当一个电子源,容易与缺电子的亲电试剂发生反应,这一性质类似于烯烃中的π键。但苯环中π键又有别于烯烃中的π键,其π键共振形成的大π键使苯环具有特殊的稳定性,反应中总是保持苯环大π键的整体结构。苯的结构特点决定苯容易发生亲电性取代反应。2
苯与氯、溴的亲电取代反应机理如下:
1、缺电子的三卤化铁与卤素结合,促进卤素σ键的极化、异裂。
FeX3+X2→X++FeX4-
2、带正电的卤离子进攻苯环的π电子,形成苯碳正离子中间体,这一步是速度决定步骤。
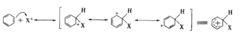
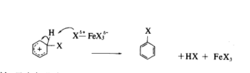
3、苯碳正离子失去一个质子形成卤代苯,同时释放卤化氢和卤化铁,卤化铁再继续起催化作用。
本词条内容贡献者为:
杨剑虹 - 教授 - 西南大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国