烷基上的C—H σ键能与处于共轭位置的π键、p轨道发生侧面部分重叠,产生类似自电子离域现象,使体系变得稳定,这种σ键的共轭称为超共轭效应。超共轭效应与π-π共轭效应,p-π共轭效应相比较,作用要弱得多。超共轭效应一般是给电子的,其大小顺序如下:一CH3>—CH2R>一CHR2>一CR3。
σ-π超共轭体系在丙烯分子中,虽然甲基中的C—H σ键轨道与π键的两个p轨道并不平行,交盖概率较小,但它们仍然可以在侧面相互交盖,如图:
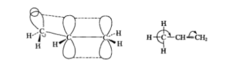
由于这种交盖,σ电子偏离原来的轨道,而倾向于π轨道。这种涉及σ键轨道与π轨道参与的电子离域作用,称为超共轭效应,亦称σ-π超共轭效应,这种体系称为超共轭体系。1
σ-π超共轭体系的形成使原来基本上定域在两个原子周围的π电子云和σ电子云发生离域而扩展到更原子的周围,因而降低了分子的能量,增加了分子的稳定性。在丙烯分子中,由于C—C单键的转动,甲基中的三个C—H σ键轨道都有可能与π轨道在侧面交盖,参与超共轭。由此可知,在超共轭体系中,参与超共轭的C—H σ键越多,超共轭效应越强。例如:
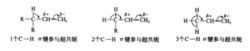
在研究有机反应时有着重要的应用,在学习不对称烯烃的HX加成反应时,我们以碳正离子形成的稳定性来解释马尔科夫尼科夫规则。若应用σ-π超共轭效应,则不仅说明甲基是推电子的,同时加深了对这一经验规则的深入理解。再如,不饱和烯烃的σ-H的特殊活泼性也可以用σ-π超共轭效应来理解。丙烯的甲基比丙烷的甲基活泼的多,在液氨中丙烯中甲基的H易被取代,丙烷中甲基的H不易被取代。
σ-p超共轭体系在碳正离子中,带正电荷的碳原子是sp2杂化,剩余的一个p轨道是空着的,存在着σ键轨道与p轨道在侧面相互交盖,称为σ-p超共轭效应。1
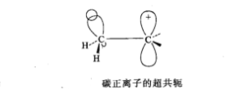
参与超共轭的C—Hσ键轨道越多,正电荷的分散程度越大,碳正离子越稳定。碳正离子稳定性从大到小是:3。C+>2。C+>1。C+>CH3+。
烷基自由基也倾向于平面结构,未成对的孤电子处于p轨道中,许多自由基中有存在着超共轭。
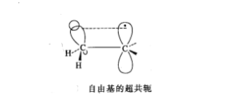
由于超共轭效应的存在,自由基得到稳定。参与σ-p超共轭的C—Hσ键轨道越多,自由基越稳定。
超共轭体系对物理特性的影响1、键长
在共轭体系中,电子云发生离域而使键长趋于平均化。超共轭效应是C—H键电子或多或少参与整个体系电子云的离域,因此也具有键长趋于平均化。
2、吸收光谱
由于超共轭效应的存在,使共轭体系中电子活动范围增大,吸收向长波方向位移。C—H键的超共轭数愈大,电子的活动范围愈大,吸收愈向长波方向位移。
3、氢化热
烯烃氢化是一个放热反应,从各种烯烃的氢化热数据可得知烯烃的相对稳定性。
4、偶极矩
在烯烃分子中如有共轭效应存在则产生电子转移的趋向,使分子内部正负电荷分散,偶极矩增大。 但诱导效应也使偶极矩增大,并且二者方向是一致的,测出的μ值应为两者之和。2
本词条内容贡献者为:
李廉 - 副教授 - 中国矿业大学




 扫码下载APP
扫码下载APP

 科普中国APP
科普中国APP
 科普中国
科普中国
 科普中国
科普中国