|
我们来自哪里?可能不是自己妈妈的子宫科普中国中央厨房 2020-07-31 |
在未来,我们或许不需要用人体来孕育生命。子宫缺失或损伤者,亦可以选择是否再造或修复子宫。但在此之前,一系列伦理问题也有待解决。
图虫创意
作者 | 祝叶华
科幻电影《黑客帝国》中展示了一个里面生长着胎儿的生物袋网络。现在,科学家正在逐渐实现这种异位妊娠(胚胎或胎儿在母亲体外的生长)的想法。子宫移植和人造子宫的辅助生殖技术正逐渐改变我们对生孩子的看法。
最近,美国科学家利用人造子宫技术产出了足月且存活的兔仔,这一技术的突破,可能会增加患有子宫功能性障碍的女性孕育后代的机会,随之而来的道德伦理也将长期存在。
01.
我们为什么需要子宫
说到人类健康,心脏通常是第一位的,其次是大脑,然后可能是消化系统,子宫这个器官可能无法挤进前三。然而,子宫在实现人类繁衍生息方面发挥着巨大的作用,它是所有生命的载体,它会导致出血和疼痛,每年让2亿妇女怀孕,并对10%到20%以流产告终的怀孕负有部分责任。
人类的子宫大致呈梨形,由韧带和肌肉固定在骨盆内。两条输卵管进入子宫的上部,即右侧和左侧的圆形末端。子宫在女性的生殖能力中有许多重要和关键的功能,它最主要的作用是为发育中的胎儿提供居所,并保护其发育成熟到足以分娩。子宫的其他作用包括参与月经产生,以及为膀胱、肠和盆骨提供结构支持。
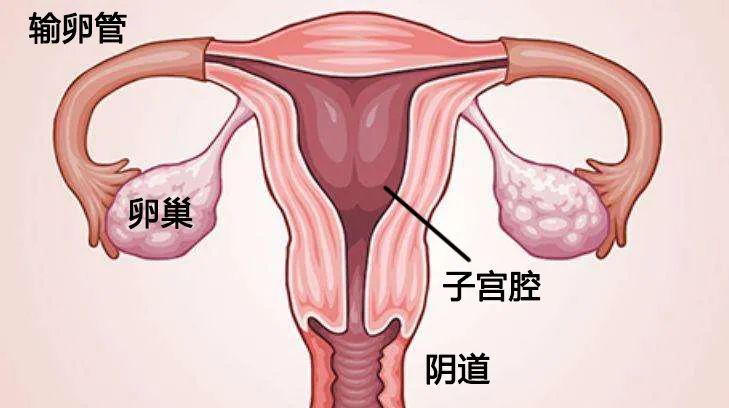
人类的子宫 | 来自网络
子宫是一个不可思议的可膨胀器官,在怀孕期间它可以从拳头大小膨胀到足以容纳一个足月的婴儿。它也是一个非常强壮的器官,能够在分娩时有力地收缩,将足月的婴儿推出体外。
子宫承担了人类繁衍生息的重任,但女性体内的这一器官有时会因各种因素,如先天性的生理原因、癌症、受伤或医疗条件而丧失其生理功能甚至是失去这一器官,更有小部分人患有无子宫症。
以无子宫症为例,有数据显示,全球大约每4500名女性中就有1名患有先天性子宫阴道缺陷综合征(MRKH),即无子宫症。在新技术出现之前,这些子宫受损或缺失的女性,想要生育后代的唯一的途径就是代孕。但在中国、挪威和瑞典的等国,法律明确禁止代孕。
02.
人造子宫的前奏:子宫移植
在人造子宫技术还停留在概念或者设计阶段的时候,子宫移植技术的发展在一定程度上重燃了患有子宫功能性障碍的女性生育后代的希望。
所谓的子宫移植,就是将子宫从一位女性身体上摘除后,移植到另一位女性(现在也有移植到男性体内的尝试)的体内。
2000年,沙特阿拉伯完成了全球首个有记录的子宫移植案例,但被移植的子宫3个月后因为血栓问题而不得不再次被移除。2014年,全球首次成功移植的子宫孕育新生命[1]。2018年世界首个已故捐献者子宫移植孕育的婴儿诞生,并健康成长[2]。2019年1月23日,我国空军军医大学西京医院召开发布会,宣布中国首例子宫移植并胚胎移植出生的婴儿诞生[3]。

2015年,一位女士接受母亲的子宫移植,于2019年诞下中国首例“添宫宝宝”。图为出生3天的宝宝。| 新京报
虽然有成功案例在前,但这项技术还不够成熟。
子宫在移植之后会在接受者体内出现排异反应,接受者要服用多种药物控制排异反应。尤其是接受子宫移植后成功怀孕的女性,在怀孕前已经服用大量免疫移植药,这些药物是否会导致婴儿早产并增加新生儿低出生体重风险尚不知晓。
除排异反应外,女性的子宫是个复杂而又纤细脆弱的器官,为它供血的只有4根非常细的血管,因此很容易产生血块凝结。
另外,由于移植手术并没有将子宫连接至输卵管,因此接受移植子宫的妇女并不能自然受孕,医生会采取卵子进行试管受精制造胚胎。
与此同时,由于子宫移植妇女需要长期服用免疫药物来防止排斥现象,所以一旦通过移植手术后生儿育女后,体内移植的捐赠子宫就必须在接受剖腹产的同时被摘除掉。这样接受者将不需要终身服用免疫抑制药,所以这种移植只能是短期的。
03.
捧过接力棒的人造子宫
鉴于子宫移植的排异反应和暂时性,人造子宫被寄予“厚望”。
其实,人造子宫的诞生在很大程度上是由大量的、持续增长的早产儿推动的。虽然医学的进步已经帮助了更多的早产儿存活下来,但是早产儿却面临着呼吸、心血管和感觉系统受损、视觉和听觉问题以及严重的学习障碍的风险。另外,出生在24周或24周以下的婴儿仍然不太可能存活。
人造子宫提出了早产儿治疗方式的革命性转变:从试图为挣扎着维持生命的早产儿提供机械帮助(侵入性尝试),转向试图通过子宫外继续妊娠来支持发育。
人造子宫的概念可以追溯到1923年,当时英国生物学家J.B.S.霍尔丹创造了“外生”一词,提出了人造子宫的设想。1992年,日本科学家尝试建立胚胎试验医学的动物模型,研制出挽救早产儿或病弱胎儿的技术。他们以羊为对象,在母羊怀孕120天后通过解剖手术取出小羊模拟早产,并利用人造橡胶子宫代替母体子宫,继续孕育小羊。随后循环衰竭和其他技术问题夺去了这只小羊的生命,实验宣布失败,但这项试验对于人造子宫的研究依然有着积极的推动作用[4]。
2017年,美国费城儿童医院研究团队打造的“人造子宫”首次通过了动物试验。研究人员制造了一个充满人造羊水(含有盐和其他电解质的温水)的聚乙烯薄膜袋来模拟母羊的子宫,通过脐带接口连接氧气,形成封闭的流体人造环境。在聚乙烯薄膜袋外,配置一台机器胎盘,胎盘的“血管”与早产小羊的脐带连通。试验中采取体外膜氧合(ECMO,即人工心/肺)系统为胎儿提供血液循环支持,因不依赖机器泵促进胎儿血液循环,所以该系统避免了早产儿抢救过程中面临的最大问题:血液循环。
试验选择了8只110天大的超早产羔羊(相当于妊娠23-24周的人类早产儿)进行测试,这是人类婴儿可以出生的最早时刻。在人造子宫中被孕育4周后,小羊出生了。多项生理指标测试结果显示,羊羔发育正常,它们可以正常吞咽和呼吸,除了部分小羊出现轻微肺部炎症外,其他小羊羔都非常健康。这一技术虽然鼓舞人心,但研究人员表示,“人造子宫”并不能完成长达9个月的孕期,这项技术还不能替代最早的胎儿生长阶段[5]。

体外人造子宫孕育小羊。|来自网络
2019年,欧盟地平线2020计划资助荷兰埃因霍温理工大学科研人员300万欧元,用于为人类制造一个人造子宫原型。埃因霍温理工大学的科研人员也描绘了新版人造子宫的设计构思,他们的人造子宫不仅仅是一个“塑料袋”,而是一个环境,在这种环境中,妊娠可以“感觉到、看到、闻到和听到与他们在子宫里时一样的声音……”。除此之外,人造子宫连接的系统还会持续监测胎儿的心率、氧气供应等情况。该研究小组希望能在5年内将这样的人造子宫投入人类临床试验[6]。
2020年,人造子宫技术在动物研究领域有了新突破,美国维克森林再生医学研究所(WFIRM)使用生物工程技术制造的子宫组织能够成功修复兔子子宫,使其产下存活后代[7]。
04.
修复受损子宫,产下足月兔仔
新研究可以说是人造子宫和子宫移植的联合。它不像之前的人造子宫一样,在体外孕育胎儿;也没有用其他个体的子宫移植,而是利用生物工程技术再造子宫。
选择兔子为实验对象,是因为与其他实验室动物相比,兔子的子宫相对较大,有两个分离的功能性子宫角和子宫颈,每个子宫角和子宫颈都有能力怀孕。
该研究的核心在于,用3D打印技术,为兔子量身定做可生物降解的聚合物支架;然后,从每只兔子的子宫组织中提取干细胞,接种到支架上,以培养人工子宫组织;最后,将兔子部分子宫切除,换上培育好的人工子宫组织。——这种培育人工组织的方法,此前在其他人造器官上也有所应用。
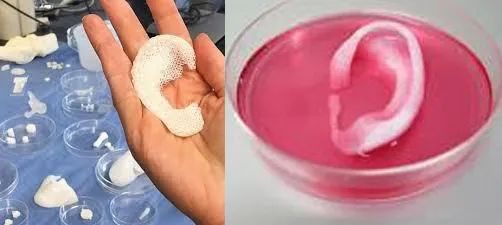
此前(同一研究机构)使用3D打印技术制作的耳形软骨,可作为细胞组织的支架,为人造器官提供结构和强度支持。|Nature Biotechnology
实验兔子被随机分成4组:(1)组织工程子宫组,切除部分子宫后,植入经过自身细胞接种的支架;(2)未接种支架组,仅植入聚合物支架;(3)部分子宫切除对照组,仅对切除部位进行缝合修复;(4)健康对照组,接受假剖腹手术。
6个月后,只有第一组兔子形成了天然的子宫组织样结构,包括有组织的腔/腺上皮、血管化的粘膜和双层子宫肌层等。也只有这一组兔子在子宫重建部分有正常妊娠,并支持胎儿发育至足月和活产,而且后代的大小和体重与正常子宫的后代相当。


人造子宫孕育兔仔的CT图像(左滑看产后照片,慎点)
不过该研究只制造了部分子宫组织,没有制造出整个子宫。并且,兔子没有月经,和人类有区别,这也是需要进一步突破的核心问题。因为子宫在人类自发的排卵和月经周期中也发生着周期性变化,在尝试用相似的方法研发人造人类子宫的时候,这个差异很可能会产生影响。
研究团队希望未来能用这种技术取代子宫移植,进而应用到人类身上。但该技术目前离临床还有一段距离。
05.
技术之外的伦理道德
尽管科学家们已经验证了子宫移植、人造子宫、半人造子宫(子宫修复)的可行性,但这并不意味着此类生殖辅助技术已经成为一项成熟的医学技术,诸多技术问题还待解决。微小血管的结构完整性、合成导管的物理限制、胎儿和胎盘之间复杂的分子交换,以及早产儿通常较差的预后,都说明了这是一项极其复杂的科学。
而随着新技术快速发展,当技术难题一一被突破的时候,人工子宫可能会使怀孕成为一种生殖选择,甚至可以被看作是一种替代的生育治疗方法,与子宫移植和代孕一起,用于那些不能完全怀孕的人。这使得我们需要在技术发展之前,仔细考虑其可能带来的法律和伦理影响。
比如,法律对胎儿和婴儿的处理非常不同,应该如何界定人造子宫(尤其是体外人造子宫)实体?人类实体中的妊娠期对此是否适用?
与这些设备的临床转化有关的问题也同样棘手。比如,在早产儿身上进行测试是否更合乎道德?技术成熟后,哪些类别的早产儿可以借助这些手段延续生命?未来新生儿先天性疾病的概率会不会因此技术的应用而有所增加?
与此同时,人造子宫可能对面临严重医疗并发症的婴儿和母亲有挽救生命的作用,但与人相比,被机器部分孕育的潜在长期后果也存在不确定性。
更为现实的一个问题是,如果有一天借由“人造子宫”出生的孩子问到:“我从哪里来?”我们应该如何讲好这个临床故事。
参考文献;
[1] https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(14)61728-1/fulltext.
[2] Dani Ejzenberg, Wellington Andraus,Luana Regina Baratelli Carelli Mendes, et al. Livebirth after uterustransplantation from a deceased donor in a recipient with uterineinfertility[J]. The Lancet, 2018, 2018, doi:10.1016/S0140-6736(18)31766-5.
[3] http://www.xinhuanet.com/politics/2019-01/23/c_1124032786.htm.
[4] Japanese pioneers raise kid in rubberwomb. New Scientist, Apr 25 1992.
[5] https://www.nature.com/articles/ncomms15112.
[6] Artificial womb: Dutch researchersgiven €2.9m to develop prototype. The Guardian, Oct 8 2019.
[7] Magalhaes, R.S., Williams, J.K., Yoo,K.W. et al. A tissue-engineered uterus supports live births in rabbits. NatBiotechnol (2020). https://doi.org/10.1038/s41587-020-0547-7).
文章由“十点科学”(ID:Science_10)公众号发布,转载请注明出处。
责任编辑:王超
 科普中国APP
科普中国APP
 科普中国微信
科普中国微信
 科普中国微博
科普中国微博

最新文章
-
为何太阳系所有行星都在同一平面上旋转?
新浪科技 2021-09-29
-
我国学者揭示早期宇宙星际间重元素起源之谜
中国科学报 2021-09-29
-
比“胖五”更能扛!我国新一代载人运载火箭要来了
科技日报 2021-09-29
-
5G演进已开始,6G研究正进行
光明日报 2021-09-28
-
“早期暗能量”或让宇宙年轻10亿岁
科技日报 2021-09-28
-
5G、大数据、人工智能,看看现代交通的创新元素
新华网 2021-09-28













微信扫一扫:分享
微信里点“发现”,扫一下
二维码便可将本文分享至朋友圈。