|
药物临床研究那些事儿中国药学会 2019-02-13 作者:北京朝阳医院药事部 杜萍 |
药物的前世
药物的前身是一种候选化合物,药理学家们对这些候选化合物进行体外(如细胞水平)和体内(如动物水平)的药理学活性筛选和评价,若其具有药学活性(即药效和安全性兼得),即可晋升为“先导化合物”。“先导化合物”具有后续开发为“候选药物”的潜力。
什么是药物临床研究?
药物临床研究是指任何在人体(健康志愿者或患者)开展的药物系统性研究,是对药物治疗效果、用药剂量、不良反应的不断探索和验证过程。
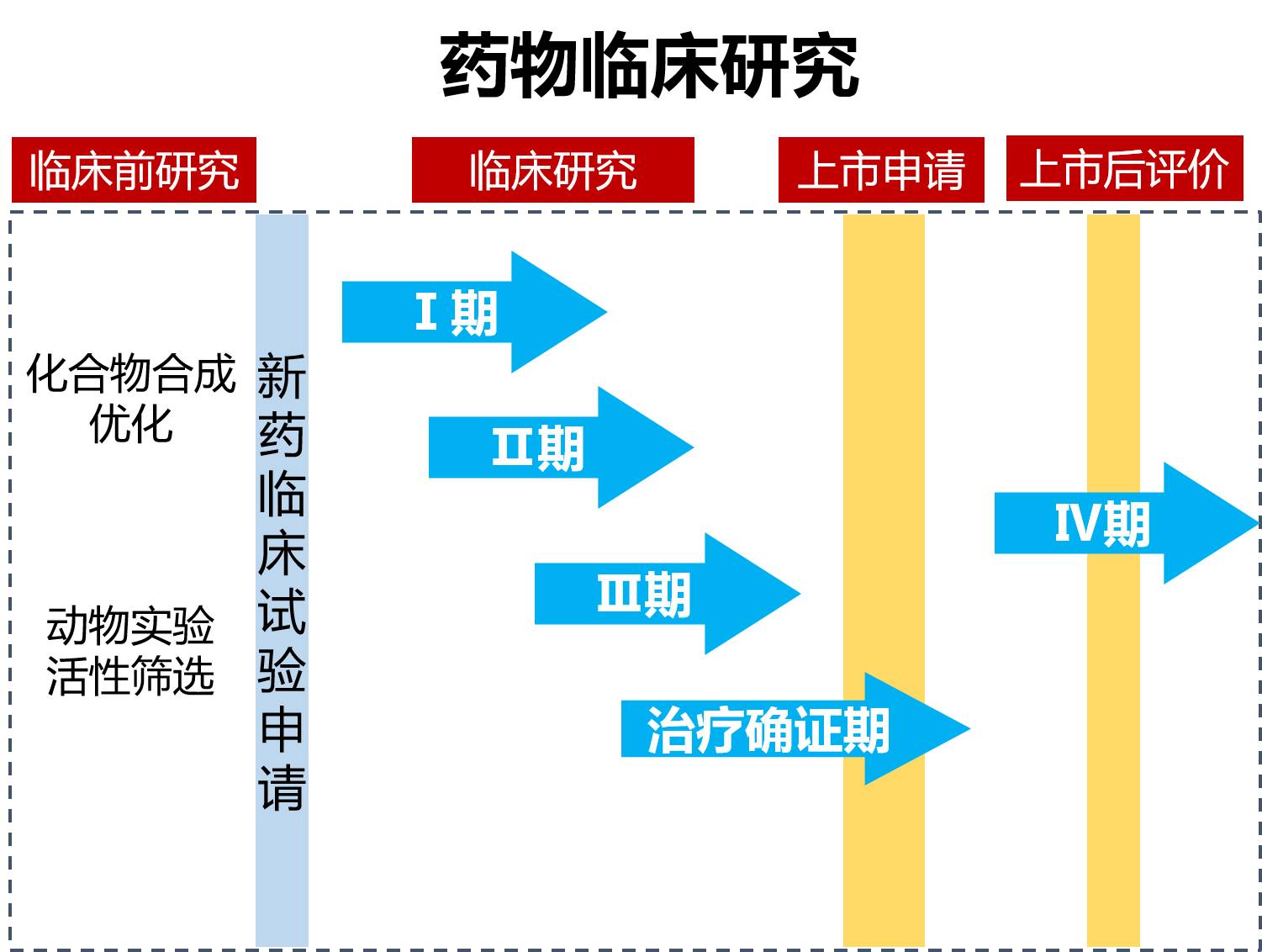
临床研究分哪些阶段呢?
临床研究根据受试人群数量及药物的特点主要分为四期,即Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期,让我们分阶段来详细了解一下吧~
1Ⅰ期临床研究
主要由健康志愿者参加,是“候选药物”首次在人体内评价的过程,人数要求一般为18至24例,在有资质的临床试验机构进行。目的是初步评价药物在人体内的安全性、观察不良反应,人体对药物剂量的耐受性,以及药物在人体的吸收、分布、代谢和排泄特征,为后续临床给药方案的制定提供依据和参考。但是一些抗肿瘤药物本身对健康志愿者造成损害,所以一些抗肿瘤药物的临床研究受试人群由肿瘤患者组成。
2Ⅱ期临床研究
由患者参与,参加人数约100人,这一阶段的目的是初步评价药物对目标适应症患者的治疗作用(如无效、改善、有效、治愈)和安全性(如不良反应),为Ⅲ期临床研究设计和给药剂量方案的确定提供依据。

3Ⅲ期临床研究
多中心研究,在多个地方进行,参加人数约300人,目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请提供充分的证据。

经过Ⅰ期、Ⅱ期和Ⅲ期临床研究后可以向国家食品药品监督管理局(CFDA)提出新药注册申请,一旦新药获得批准生产就可以在市场上购买了。新药从最初的实验室研究到批准上市大约需要10余年的时间。
4Ⅳ期临床研究
新药上市后进行的应用研究阶段,其目的是考察广泛使用条件下药物的疗效和不良反应,评价的周期较长,最终权衡药物的长期获益和风险。

希望通过小编的整理您能够更加了解上市药品的来之不易,体会药学科研工作者的良苦用心,更加安全合理的使用药物!
作者:杜萍 北京朝阳医院药事部
编辑:刘莹 北京朝阳医院药事部
注:部分图片来自网络
责任编辑:王超
上一篇:下肢深静脉血栓知多少
下一篇:最美口服降糖药的跟踪报道
 科普中国APP
科普中国APP
 科普中国微信
科普中国微信
 科普中国微博
科普中国微博

最新文章
-
为何太阳系所有行星都在同一平面上旋转?
新浪科技 2021-09-29
-
我国学者揭示早期宇宙星际间重元素起源之谜
中国科学报 2021-09-29
-
比“胖五”更能扛!我国新一代载人运载火箭要来了
科技日报 2021-09-29
-
5G演进已开始,6G研究正进行
光明日报 2021-09-28
-
“早期暗能量”或让宇宙年轻10亿岁
科技日报 2021-09-28
-
5G、大数据、人工智能,看看现代交通的创新元素
新华网 2021-09-28